Thu hồi toàn quốc thuốc Navacarzol 5mg trị bệnh tuyến giáp
13:04 | Chủ nhật, 26/07/2020 0Cục quản lý Dược (Bộ Y tế) vừa có thông báo thu hồi toàn quốc thuốc viên nén Navacarzol 5mg (Carbimazole 5mg), SĐK: VN-17813-14, Số lô: 180513/2, NSX: 11/2018, HD: 10/2021 do Công ty Industria Farmaceutica Nova Argentia S.p.A (Italy) sản xuất, Công ty cổ phần dược phẩm Thiên Thảo nhập khẩu.
Lô thuốc viên nén Navacarzol 5mg bị thu hồi có mẫu thuốc kiểm nghiệm không đạt tiêu chuẩn chất lượng về chỉ tiêu độ dày, độ cứng, độ hòa tan, định lượng (vi phạm mức độ 3).
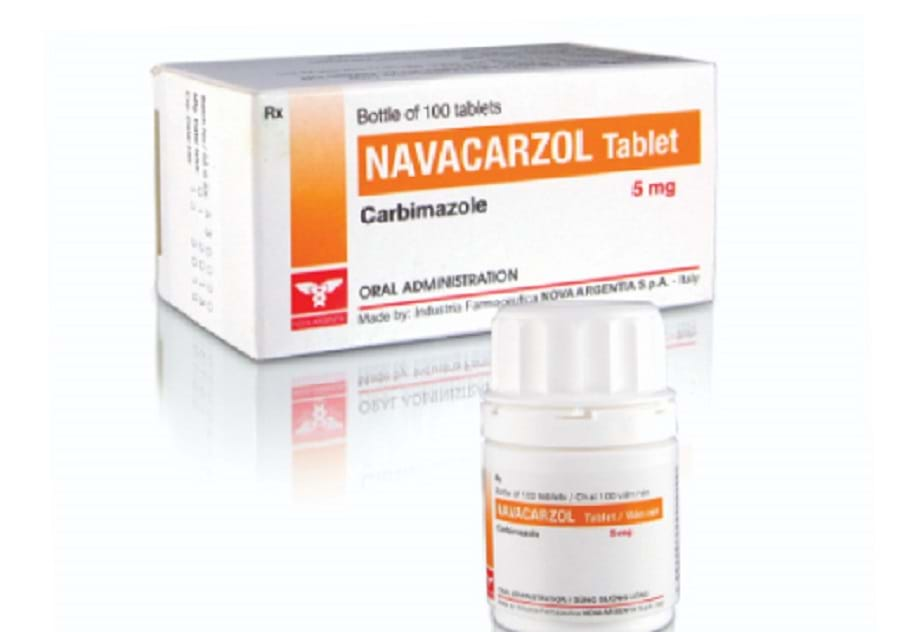
Ảnh minh họa
Công ty Thiên Thảo phối hợp với nhà cung cấp và nhà phân phối thuốc phải trong thời hạn 2 ngày kể từ ngày 24.7 gửi thông báo thu hồi tới các cơ sở bán buôn, bán lẻ, sử dụng viên nén Navacarzol 5mg (Carbimazole 5mg), SĐK: VN-17813-14, Số lô: 180513/2, NSX: 11/2018, HD: 10/2021 do Công ty Industria Farmaceutica Nova Argentia S.p.A (Italy) sản xuất, Công ty Thiên Thảo nhập khẩu và tiến hành thu hồi toàn bộ lô thuốc không đạt tiêu chuẩn chất lượng nêu trên.
Báo cáo thu hồi gửi về cục quản lý dược trong vòng 18 ngày kể từ ngày 24.7, hồ sơ thu hồi bao gồm số lượng nhập khẩu, ngày nhập khẩu, số lượng thu hồi, các bằng chứng thực hiện thu hồi tại các cơ sở bán buôn, bán lẻ, sử dụng đã mua thuốc theo quy định của Bộ Y tế về chất lượng thuốc và nguyên liệu làm thuốc.
Sở y tế các tỉnh, thành phố trực thuộc trung ương, y tế các ngành thông báo cho các cơ sở kinh doanh, sử dụng thuốc thu hồi lô thuốc không đạt tiêu chuẩn chất lượng nêu trên;
Công bố thông tin về quyết định thu hồi thuốc trên trang thông tin điện tử của sở; kiểm tra và giám sát các đơn vị thực hiện, xử lý những đơn vị vi phạm theo quy định hiện hành, báo cáo kết quả về Cục quản lý Dược và các cơ quan chức năng có liên quan.
Sở y tế Hà Nội kiểm tra và giám sát Công ty Thiên Thảo thực hiện việc thu hồi và xử lý thuốc bị thu hồi theo quy định.
Thuốc viên nén Navacarzol 5mg được dùng trong điều trị một số rối loạn tuyến giáp đi kèm với cường giáp.
Minh Hoàng
- TP.HCM dự kiến khởi công 10 dự án hơn 381.000 tỷ đồng nhân kỷ niệm 50 năm thành phố mang tên Bác
- Nếu phương tiện bị hỏng do sử dụng E10, ai sẽ chịu trách nhiệm?
- VinFast hợp tác NVIDIA và Autobrains triển khai chương trình taxi tự lái cấp độ 4 thế hệ mới cho thị trường Đông Nam Á
- TP.HCM tính chuyện 100 năm: Xây siêu đô thị toàn cầu với 5 cực tăng trưởng
- TP.HCM phác họa tầm nhìn 100 năm: Siêu đô thị đa trung tâm, kết nối biển, dẫn dắt tăng trưởng khu vực
- Câu chuyện tháng Tư với gia đình anh Bảy
- Không gian thoát lũ sông Hồng: giới hạn hay cơ hội của Hà Nội?
- Hà Nội trong vòng xoáy “đập đi xây lại”: Ô nhiễm và nỗi lo mất bản sắc
- Nghiêu Đề - lặng lẽ tài hoa
- Những bến tàu xưa thành công viên kỳ thú
- Đi tìm sức sống đô thị
- Thành phố đi xa... hay con người đi lạc?
- TP.HCM: Giám sát khảo cổ học khi thi công móng Nhà văn hóa Thanh niên
- Chuyến về Sài Gòn thăm nguồn cội của hậu duệ chú Hỏa
- Gia tộc chú Hỏa góp công lớn tạo nền móng đô thị Sài Gòn


